はじめに
OpenAIが2025年12月16日、GPT-5が実験室での生物学研究を加速できることを実証したと発表しました。分子クローニングプロトコルの効率を79倍に改善し、新しい酵素メカニズムを提案したとのことです。本稿では、この発表内容をもとに、AIによる実験最適化の仕組みと可能性について解説します。
参考記事
- タイトル: Measuring AI’s capability to accelerate biological research in the wet lab
- 著者: Nikolai Eroshenko, Miles Wang, Rachel Smith, Liliana Abramson, Tejal Patwardhan, Kemo Jammeh, Chase Olle, Azadeh Samadian, Nitin Mahadeo
- 発行元: OpenAI
- 発行日: 2025年12月16日
- URL: https://openai.com/index/accelerating-biological-research-in-the-wet-lab/
要点
- GPT-5は、分子クローニングプロトコルの効率を79倍に改善した
- RecAとgp32という2つの酵素を組み合わせた新しいメカニズム「RAPF-HiFi」を提案した
- 人間の介入は実験の実施とデータ入力のみで、プロトコルの提案と分析はGPT-5が自律的に実施した
- 複数ラウンドの実験を通じて反復的に学習し、改善案を提示した
- ロボットシステムとの統合により、自然言語のプロトコルを実際の実験に変換することにも成功した
詳細解説
GPT-5による実験最適化の仕組み
OpenAIは、バイオセキュリティ企業Red Queen Bioと協力して、GPT-5が実験室での提案、分析、反復をどのように行うかを評価する枠組みを構築しました。実験システムとして、緑色蛍光タンパク質(GFP)遺伝子とpUC19プラスミドを用いた2ピースクローニング反応を設定し、成功したコロニー数を増やすことを目標としました。
GPT-5は各ラウンドで8-10種類の異なる反応を提案し、人間の研究者がそれらを実行してコロニー数を測定しました。最も性能の良いデータが次のラウンドに引き継がれ、GPT-5はそれをもとに新たな改善案を提示するという流れです。重要なのは、プロンプトが標準化されており、人間による誘導がなかったという点です。これにより、新しいメカニズムの発見がGPT-5自身によるものであることが示されました。
このアプローチは、実験的な検証が必要な生物学分野において、AIがどのように研究を支援できるかを示す試みと言えます。数学や理論物理学のように厳密な検証が可能な分野とは異なり、生物学では実験的な実行と経験的な検証が不可欠であるためです。
79倍の効率改善と新しい酵素メカニズム
OpenAIによれば、GPT-5は複数ラウンドの最適化を通じて、クローニング効率を79倍に改善しました。これは、同じ量の入力DNAから、ベースラインプロトコルと比較して79倍多くの配列検証済みクローンが得られたことを意味します。
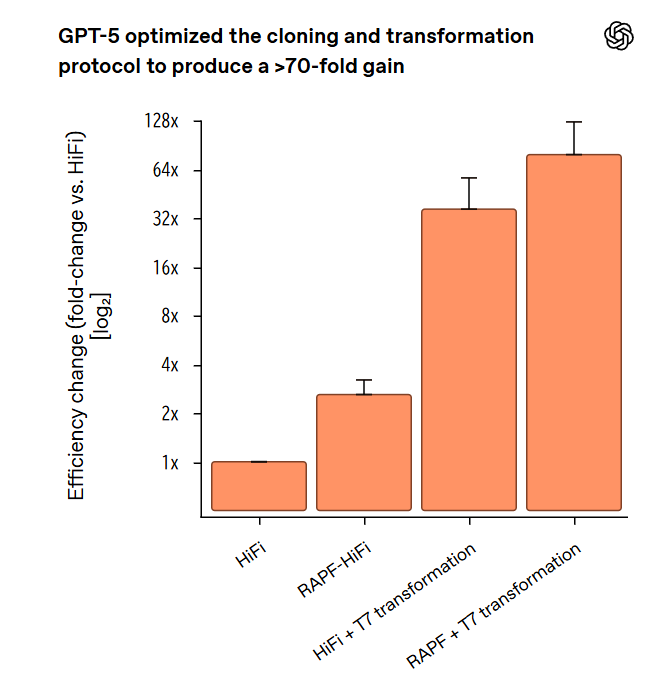
最も注目すべき点は、GPT-5が「RAPF-HiFi(RecA-Assisted Pair-and-Finish HiFi Assembly)」と呼ばれる新しい酵素メカニズムを提案したことです。このメカニズムは、大腸菌由来のリコンビナーゼRecAと、ファージT4の遺伝子32由来の一本鎖DNA結合タンパク質(gp32)という2つの酵素を組み合わせたものです。
gp32はDNAの緩んだ末端を滑らかにほどき、RecAは各鎖を正しい相手に導く役割を果たします。この2つのタンパク質が協調して働くことで、DNAの相同性検索と結合が促進されると考えられます。従来のGibsonアセンブリでは、DNAの末端を短時間加熱して相補的な配列が結合できるようにしていましたが、RAPF-HiFiではより効率的なマッチングが可能になったと推測されます。
この効率改善は、タンパク質工学、遺伝子スクリーニング、生物株の改変などに用いられる大規模で複雑なライブラリの作成において重要な意味を持つと考えられます。
変換プロトコルの最適化
クローニング反応の最適化と並行して、GPT-5は変換(transformation)手順も最適化しました。OpenAIの発表では、13種類の異なるプロトコルを一度にテストする「ワンショット」ラウンドが実施されました。
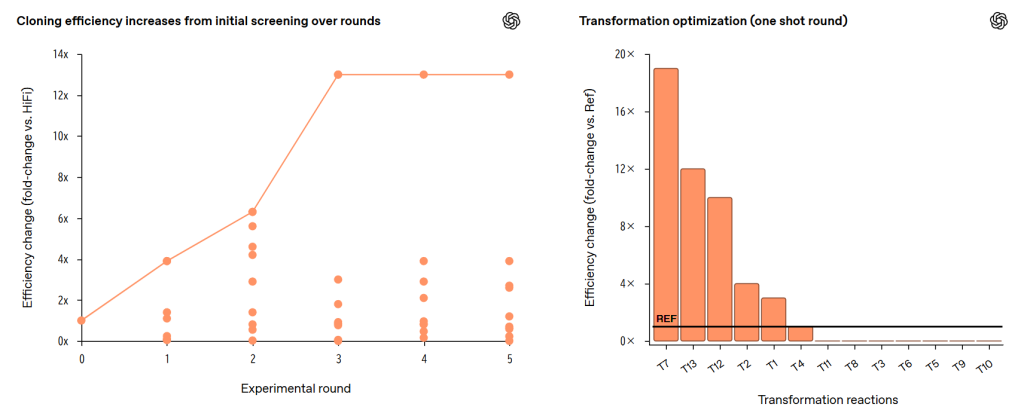
最も効果的だった「Transformation 7(T7)」は、意外にもシンプルな改変でした。細胞をペレット化(遠心分離で底に集める)し、供給された体積の半分を除去してから細胞を再懸濁し、すべて4℃で実施するというものです。OpenAIによれば、高効率の化学的コンピテント細胞は通常デリケートと考えられており、このような取り扱いは一般的に避けられていますが、細胞は濃縮に耐え、分子衝突の増加により変換効率が大幅に向上したとのことです。
この変換プロトコルの改善により、30倍以上の効率向上が達成されました。クローニング反応の2.6倍改善と組み合わせることで、最終的に79倍の総合的な効率改善につながったと説明されています。
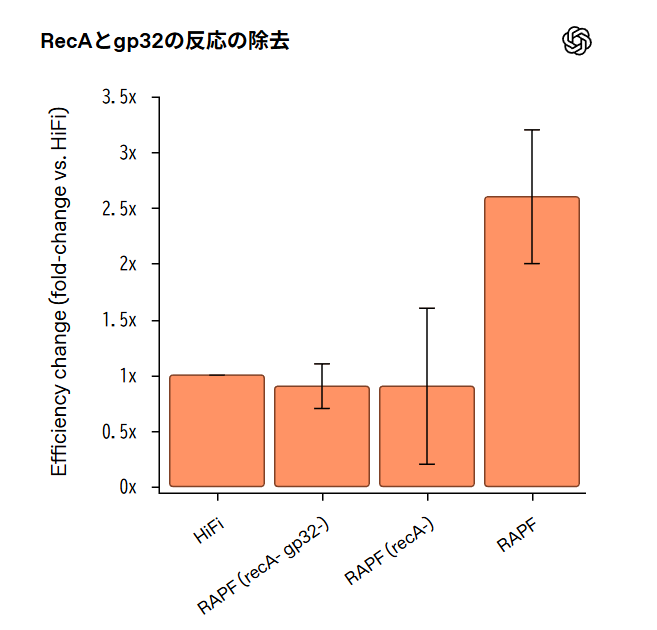
RecAとgp32の組み合わせは新規か
OpenAIの発表では、RecAとgp32の機能的な組み合わせは、分子生物学の手法としてはこれまで知られていなかったとされています。ただし、基礎となる生化学的活性自体はすでに研究されていました。
例えば、Dループ形成の研究において、gp32がRecA活性を高めることが示されています。また、gp32は天然のT4リコンビナーゼパートナーであるUvsXやuvsYと組み合わせて、リコンビナーゼポリメラーゼ増幅(RPA)で使用されてきました。しかし、RecAとgp32を実用的で一般化可能な手法として組み合わせたのは、今回のGPT-5の提案が初めてである可能性があります。
OpenAIは、多くの新しい分子生物学技術と同様に、基礎となる生化学的活動はすでに研究されていたものの、それらを実用的で一般化可能な手法として使用することが進歩であると説明しています。
従来のGibsonスタイルのDNA組み立て反応への改善は少なく、最も注目すべき例は熱安定性DNA結合タンパク質(ET SSB)による約2.5倍の効率改善とされています。RAPF-HiFiの2.6倍という改善は、この水準に近いものと言えます。
ロボットシステムとの統合
OpenAIは、Robot on RailsおよびRed Queen Bioと協力して、自然言語のクローニングプロトコルを受け取り、実験室で実行するロボットシステムを構築しました。このシステムは3つのコンポーネントで構成されています。
1つ目は、平易な英語をロボットのアクションに変換する「人間対ロボットLLM」です。2つ目は、実験器具をリアルタイムで識別して位置を特定するビジョンシステムです。3つ目は、各アクションを安全かつ正確に実行する方法を決定するロボット経路プランナーです。
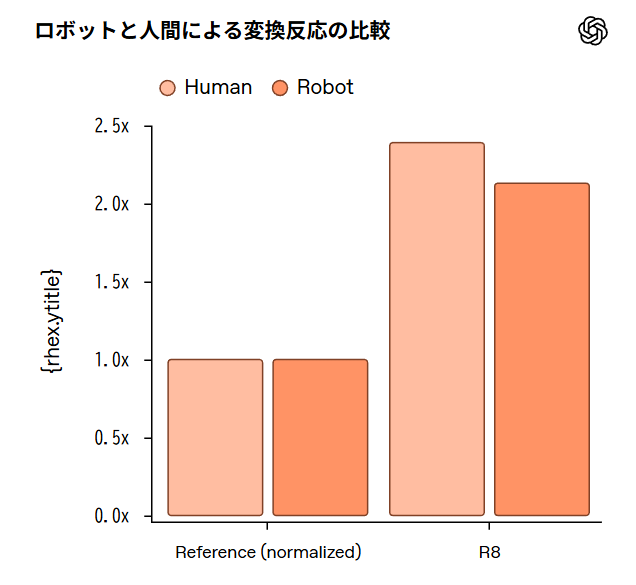
OpenAIによれば、自律ロボットが標準的なHiFi法と、最初の最適化ラウンドで最も性能の良かったR8プロトコルを同時に実行し、人間が実行した実験と比較されました。ロボットは変換プロセスを成功裏に処理し、液体の移動と混合、サンプルチューブの移動、細胞への制御された加熱、成長プレートへの細胞の塗布など、多様な物理的操作を実行しました。
OpenAIの発表では、ロボットと人間が実行した変換を直接比較したところ、ロボットは同様の品質のデータを生成し、ベースラインに対して同等の改善を示したとされています。ただし、ロボットからの絶対的なコロニー数は人間の実行よりも約10分の1低く、液体取り扱いの精度、温度制御の較正、手動細胞取り扱い技術のニュアンスの再現など、改善の余地があることも示されました。
バイオセキュリティへの配慮
OpenAIは、生物学的推論の進歩がバイオセキュリティに影響を及ぼす可能性があることを認識し、この研究を厳重に管理された環境で実施しました。具体的には、無害な実験システムの使用、タスクの範囲の制限、モデルの動作評価によるバイオセキュリティリスク評価の実施、モデルレベルおよびシステムレベルの保護措置の開発などが行われました。
OpenAIの「準備フレームワーク(Preparedness Framework)」に従い、モデルが実験室で推論してプロトコルを改善できることを示す今回の評価結果は、バイオセキュリティに関する影響を持つ可能性があるとされています。OpenAIは、これらのリスクを軽減するために必要かつ微妙な保護措置をモデルとシステムのレベルで構築し、現在のレベルを追跡するための評価を開発することにコミットしていると述べています。
まとめ
OpenAIによるGPT-5の実験室実験は、AIが生物学研究の実験プロトコル最適化を支援できる可能性を示しました。79倍の効率改善と新しい酵素メカニズムの提案は、AIが単なる文献検索や理論的推論にとどまらず、実験的な発見にも貢献できることを示唆しています。一方で、バイオセキュリティへの配慮や、人間の監視の必要性など、慎重に扱うべき課題も明らかになりました。今後、AIと人間の研究者がどのように協働していくのか、注目されるところです。









